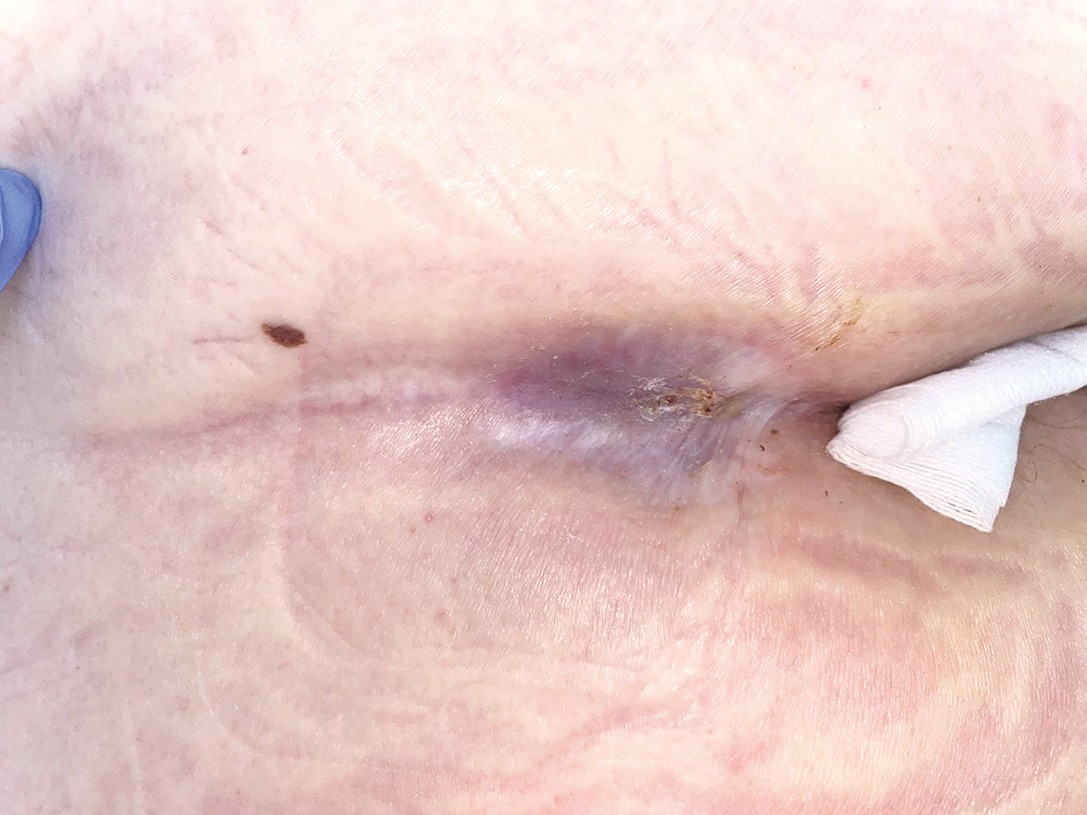
Anwendung bei einem Dekubitus Kategorie IV
Chronische Wunden verursachen einen hohen Leidensdruck und schränken die Lebensqualität der betroffenen Patientinnen und Patienten stark ein. Die Behandlung ist oft schwierig. Ein wichtiges Problem stellt hierbei oft die vorliegende bakterielle Besiedlung in Form von Biofilmen auf den Wunden dar. Denn in einem Biofilm eingebundene Bakterien verfügen über eine hohe Toleranz gegen die ansonsten hoch effektiven und bewährten Wunddesinfektionsmittel. Deshalb ist es um so wichtiger, den Biofilm zu entfernen – am besten sanft und gewebeschonend. Die Mikrowasserstrahl-Technologie kann hier für ein sehr schonendes, aber dennoch hoch effektives Débridement und ein gut präpariertes Wundbett sorgen.
SEBASTIAN KRUSCHWITZ

Sebastian Kruschwitz, Wundexperte/Pflegetherapeut Wunde ICW, Pflegefachkraft für außerklinische Beatmung, Berlin
Neben der Behandlung der Grundursachen stellt ein sauberes Wundbett eine Grundvoraussetzung für einen ungestörten Ablauf der komplexen Wundheilungsprozesse dar. So beschreibt das internationale Konsensus Dokument1 in vier Schritten die strategische Vorgehensweise zur Wundhygiene1:
1. Schritt: Spülung und Reinigung,
2. Schritt: Débridement,
3. Schritt: Die Wundrand- und Umgebungsbehandlung,
4. Schritt: Den Wundverband.
Wenn eine Wunde schwer heilt, ist die Unterbrechung des Heilungsprozesses größtenteils auf das Vorhandensein eines in der Wunde enthaltenen hartnäckigen Biofilms (zähe, dünne Schleimschicht oder Matrix mit eingebetteten verschiedenen Mikroorganismen) zurückzuführen. Obwohl auch andere patientenbedingte Faktoren die Heilung verzögern können, wird zunehmend anerkannt, dass der Großteil chronischer Wunden Biofilm enthält, der ein wesentliches Hindernis für die Heilung darstellt.
Der Biofilm als Wegbereiter einer kritischen Kolonisation erhöht das Infektionsrisiko in jedem Gewebe. Ein erhöhtes Risiko für die Bildung eines Biofilms besteht bei chronischen Wunden auf der Basis von Grunderkrankungen wie bspw. Diabetes mellitus, chronischer venöser Insuffizienz (CVI) oder peripherer arterieller Verschlusskrankheit (PAVK). Eine erhöhte mikrobielle Virulenz, Antibiotikaresistenz und/oder Immundefizit oder Immunsuppression der Patientinnen und Patienten vervielfacht nochmals das Risiko für eine Biofilmbildung. Aber auch pflegerelevante Faktoren können für eine gestörte Wundheilung verantwortlich sein, wie dem anschließenden Fallbericht zu entnehmen ist.
Kasuistik
Eine bettlägerige 61-jährige Patientin litt unter einem Dekubitalgeschwür Grad IV, das gemäß Best-Practice-Wundbehandlung nicht mehr rein ambulant versorgt werden konnte, sondern zur chirurgischen Versorgung eine Krankenhauseinweisung erforderlich machte. Bei dieser Patientin lagen folgenden Diagnosen vor:
- Wachkoma bei Stammganglienblutung rechts
- Ventrikeleinbruch bei arteriovenöser Malformation (AVM)
- Diabetes mellitus Typ 2
- schwere Dysphagie
- Arterieller Hypertonus
- Hypercholesterinämie
- pflegerelevante Komponenten: Inkontinenz Harn und Stuhl schwere kognitive Funktionsstörungen.
Zusammengefasst waren bei der Patientin nachfolgende erschwerende pflegerelevante und Wundheilung-beeinflussende Faktoren festzustellen:
- Alter
- geschwächter Immunstatus
- Kachexie
- konsumierende Grunderkrankung
- Kognitive Einschränkungen
- vollständig immobil
- Harn-und Stuhlinkontinent
- Kausaltherapie:
- im Bett ein Umlagerungssystem
- Mobilisation in den Rollstuhl (mit AD-Kissen).
Die Patientin wurde in ein Berliner Klinikum zum chirurgischen Débridement des Dekubitus eingewiesen, da sich am Wundgrund mehrere Nekrosen und avitales Gewebe gebildet hatten.
„Background: Proper debridement of the wound base is critical to facilitate wound granulation and closure in non-healing diabetic foot ulcers (DFUs). A unique micro water jet device has been developed that precisely cleans acute and chronic wounds in a tissue-preserving manner while performing a precise mechanical cleaning and stimulation of the wound base to enhance granulation and healing. In this trial the device was used to treat non healing DFUs.”1
„Conclusion: The micro water jet device was able to statistically significantly close more refractory DFUs over 16 weeks, with a significant difference in wound area reduction that should be noted. Further evaluation with larger randomized controlled trials are warranted to validate these initial promising findings.“1
Abb. 1: Zustand des Dekubitus nach dem chirurgischen Débridement in einem Berliner Klinikum.
Abb. 2: Nach Anwendung des Debritoms wesentlich weniger Beläge am Wundgrund erkennbar.
Abb. 3: Moleculight®-Aufnahme: Keine Staphylokokken oder Pseudomonas aeroginosa erkennbar.
Abb. 4: Sauberer Wundgrund: Das Granulationsgewebe hat deutlich zugenommen und füllt die Wunde aus.
Abb. 5: Die Wunde ist vollständig ausgefüllt, die Epithelisation ist in vollem Gange. Hier kam nur noch ein PU-Schaum zum Einsatz der alle 3 Tage und bei Bedarf gewechselt wurde.
Abb. 6: Vollständig epithelisierte Wunde.
Erfolgreicher Einsatz eines gebündelten Mikrowasserstrahls
Jedoch zeigte sich der Wundgrund auch nach dem chirurgischen Débridement noch deutlich belegt (Abb. 1). Um möglichst gewebeschonend zu reinigen und den verbliebenen bzw. wieder in Entstehung begriffenen, zähen Biofilm zu entfernen, setzten wir die sogenannte Mikrowasserstrahl-Technologie (debritom+, Fa. Medaxis) ein. In einer kontrollierten, multizentrischen Studie wurden die Vorteile des Débridements mittels Mikrowasserstrahl-Technologie gegenüber eines chirurgischen Standarddébridements bereits belegt.2 Das sanfte Entfernen von infiziertem, geschädigtem oder abgestorbenem Gewebe mit dem Debritom bewirkte auch bei unserem Einsatz ausgezeichnete Heilungsergebnisse. So sind nach Anwendung des Debritoms wesentlich weniger Beläge am Wundgrund erkennbar (Abb. 2).
Die Wunde wurde insgesamt 4-mal mit dem Debritom behandelt. Nach jeder Behandlung konnte man bereits sehen, dass der Wundgrund deutlich mehr gereinigt werden konnte und die Wundheilungsprozesse weiter fortschritten (Abb. 3–6).
Die Wundversorgung erfolgte mit einem Alginat als Wundfüller. Als Abdeckung wurde ein Superabsorber so lange eingesetzt, bis das Granulationsgewebe die Wunde vollständig ausfüllte. Im späteren Verlauf kam dann ein PU-Schaum zum Einsatz. Die Verbandwechselintervalle lagen bei drei Tagen. Insgesamt dauerte die Wundheilung bis zu 10 Monate, welches allerdings auch dem herabgesetzten Allgemeinzustand und den weiteren oben beschriebenen, begleitenden heilungshemmenden Faktoren zuzuschreiben war.
Autor:
Sebastian Kruschwitz, Fachbereichsleitung Wundmanagement, Pflegetherapeut Wunde ICW, Pflegefachkraft für außerklinische Beatmung, stellv. Case Manager,
ZBI-Gruppe, Franz-Jacob-Straße 4D, 10369 Berlin.
___________
1 International Consensus Document: Defying hard-to-heal wounds with an early antibiofilm intervention strategy: wound hygiene. JWC 2020; 29(3): S2–S26
2 Armstrong DG, Zelen C: Multicenter, Randomized Controlled Clinical Investigation Evaluating a Unique Micro Water Jet Technology Device Versus Standard Débridement in the Treatment of Diabetic Foot. Diabetes 2022; 71(Supp_1). DOI: 10.2337/db22-30-LB