Adrian Gillissen
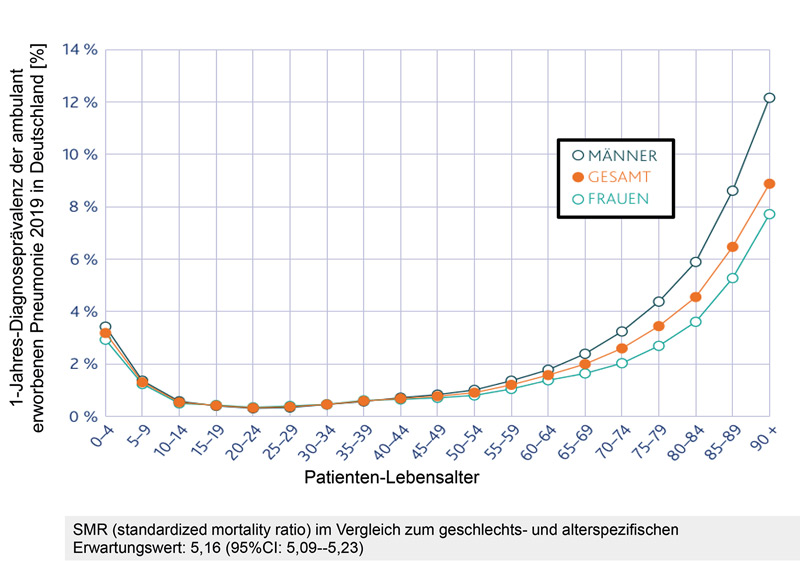
In Deutschland erkranken ca. 1,2 Millionen Menschen jährlich (Diagnoseprävalenz 2019: 1,5%) an einer ambulant erworbenen Pneumonie (CAP). Sie ist eine potenziell tödlich verlaufende Erkrankung, deren Altersgipfel im Kleinkindalter und im Senium liegt. Die Sterblichkeit gemessen als‚ standardized mortality ratio‘ (SMR) liegt bei den Betroffenen in Deutschland um etwa das fünffache über der gleichaltrigen, gesunden Bevölkerungsgruppe (Abb. 1).6

Prof. Dr. med. Dr. rer. medic. Adrian Gillissen, Med. Klinik III, Kreiskliniken, Reutlingen
Die Pneumonie wird meistens durch Viren oder Bakterien verursacht, wobei der Schweregrad der Erkrankung, der Verlauf und die Prognose in Abhängigkeit von dem Erregerspektrum und dem Risikoprofil der Betroffenen sehr variabel sind.1, 2 Folgende Faktoren sind mit einem schweren Erkrankungsverlauf und einer erhöhten Sterblichkeit assoziiert:3, 4
- Alter > 65 Jahre
- Notwendigkeit einer intensivmedizinischen Betreuung
- Immunsuppression (z. B. erkrankungs- oder Medikamenten-bedingt)
- Begleitender infektiöser Pleuraerguss/Pleuraempyem
- Nosokomial erworbene Pneumonie (HAP)5
- Schwere Grunderkrankung, wie z. B. Diabetes mellitus, kardiovaskuläre
- Erkrankungen
- Versagen der initialen antimikrobiellen Therapie
- Sepsis.
Rationale für eine systemische Kortikosteroidtherapie bei schwerer CAP
Ungefähr 40% aller CAP-Patienten werden krankenhauspflichtig, und 5% müssen sogar mit einer schweren CAP (sCAP) z. B. wegen einer respiratorischen Insuffizienz, einem Organversagen oder einer Vasopressoren-pflichtiger Hypotension (Schock) intensivmedizinisch betreut werden.3, 7, 8 Pathophysiologisch ist die sCAP durch eine lokale und systemische Inflammation mit erhöhten Blutentzündungsmarkern (z. B. CRP, Leukozyten, Procalcitonin) und einer Erhöhung von Zytokinen im Lungenparenchym und den Atemwegen (z. B. Anstieg von Interleukinen, Tumornekrosefaktor(TNF)-α, Interferon-γ im Sputum und Plasma) charakterisiert, die wiederum positiv mit dem erhöhten Letalitätsrisiko korrelieren.9 In zahlreichen Studien wurde daher versucht, mit einem antiinflammatorischen Ansatz unter Verwendung von Steroiden (Hydrokortison, Prednisolon, Methylprednisolon und Dexamethason) diese Entzündung zu inhibieren und damit das Letalitätsrisiko zu senken. Die Studienergebnisse waren aber uneinheitlich.
Die klinisch-wissenschaftliche Studienlage
Die PubMed-Suche zu dem Stichwort „severe community acquired pneumonia and steroids“ erbrachte 203 Artikel (28.01.2024). Von herausragender praktischer Bedeutung ist die Senkung der Pneumonie-Letalität. Insgesamt waren die Studienergebnisse diesbezüglich aber leider different, denn manche berichten von einem positiven Steroideffekt10, andere waren negativ.11 Zudem wird die Vergleichbarkeit der Studien und Metaanalysen durch die vielen möglichen Einflussfaktoren, wie der Charakteristik der Patienten (z. B. Alter, Begleiterkrankungen, Begleittherapie), der therapeutischen Intervention (z. B. Kortisonpräparat, Dosis, Therapiedauer) und unterschiedliche Endpunkte (z. B. Beobachtungszeitraum, ab dem der Endzeitpunkt bewertet wird) erschwert. Die 01/2024 publizierte Metaanalyse von Cheema et al. ist zu dem Thema die neueste und berücksichtigte randomisierte klinische Studien (RCTs) mit dem primären Endpunkt der 30-Tage-CAP-Mortalität.12 Eingeschlossen wurden 15 RCTs von 1972 bis 2023 mit insgesamt 3.252 Patienten. Neun Studien schlossen nur sCAP- und je drei Studien leichte CAP bzw. gemischt CAP und sCAP Patienten ein. Demnach ließ sich durch Kortikosteroide die Mortalitätsrate signifikant senken (RR 0,69, 95%CI: 0,53–0,89, p = 0,004) bei niedriger Heterogentiät (I2 = 12%). Zudem war die Krankenhausliegezeit und die Liegezeit auf der Intensivstation in der steroidfreien Gruppe signifikant länger, als die mit Steroiden (-2,35 Tage, 95%CI: -3,70–1,00, p < 0,001; respektive -1,45 Tage, 95%CI: -2,51–0,39, p = 0,007). Weitere Vorteile errechneten sich für die Steroid -Therapiegruppe durch die signifikant niedrigere Notwendigkeit einer künstlichen Beatmung, der Anzahl an Therapieversager und der Notwendigkeit zur Vasopressorentherapie. Die ARDS(adult respiratory distress syndrome)-Inzidenz blieb in beiden Gruppen gleich und als einzige signifikante Nebenwirkung wurden Hyperglykämien beobachtet.
Ganz wichtig für die Beurteilung und Interpretation der oben genannten positiven Effekte sind aber die Subgruppenanalysen:
- Die Effekte beruhten auf der Therapie nur mit Hydrokortison. Bei den anderen Kortikosteroiden errechneten sich keine signifikanten Therapievorteile.
- Signifikant ließ sich die Mortalität nur bei den sCAP-Patienten senken, nicht bei denjenigen, die eine nicht -intensivpflichtige CAP hatten.
- Die positiven Kortisoneffekte waren unabhängig von der gewählten Dosis sowie der Therapiedauer, betrafen die jüngeren Patientengruppen und gingen mit zunehmendem Alter gegen Null.12
- Die Metaanlayse unterstützt die Ergebnisse einer anderen 2023 publizierten Analyse13, steht aber im Widerspruch zu einer weiteren.14
Empfehlungen der Leitlinien
Im Gegensatz zu anderen infektionsassoziierten Krankheitsbildern wie der COPD-Exazerbation, der bakteriellen Meningitis, der ZNS-Tuberkulose oder dem septischen Schock, sind Kortikosteroide bei der leichten CAP und schweren Influenza-Erkrankungen nicht empfohlen. Bei der sCAP sind die Empfehlungen aber uneinheitlich.15 So lehnt z. B. die ATS(American Thoracic Society)-CAP-Leitinie3 den Steroideinsatz bei der sCAP ab, nicht jedoch z. B. die ERS (European Respiratory Society).4 Die DGP-Leitlinie (Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin) empfiehlt mit Verweis auf noch ausstehende Studien die Gabe von
- Hydrocortison bei sCAP im septischen Schock bei fehlendem Ansprechen auf Volumen- und Katecholamingabe,
- Systemische Kortikosteroide bei der Pneumonie-bedingten, Asthma- oder COPD-Exazerbation über 5–7 Tage (unabhängig vom auslösenden Erreger), aber
- keine generelle Steroidgabe bei hospitalisierten nicht-intensivpflichtigen CAP-Patienten und auch keine bei der schweren Influenza-Pneumonie.1
Die Society of Critical Care Medicine (SCCM) publizierte 01/2024 eine eigene sehr detaillierte Leitlinie zur Anwendung systemischer Kortikosteroide bei der Sepsis, dem ARDS und der CAP mit konkreten Empfehlungen zum vorgeschlagenen Kortisonpräparat, der Dosis und Therapiedauer:8
- Sepsis und septischer Schock: Empfehlung zur Gabe von Hydrokortison (200mg i.v./Tag als Dauergabe oder als Bolus alle 6h) mit oder ohne Fludrocortison (50µg enteral über 7 Tag oder bis Verlegung von der Intensivstation)
- ARDS: Empfehlung zur Gabe von Methylprednisolon (Beginn mit 1mg/kg/d als i.v. Bolus) oder Dexamethason (Beginn mit 20mg/Tag) bei frühem ARDS oder Methylprednisolon (Beginn mit 2mg/kg/d i.v. Bolus alle 6h) bei fehlender Besserung, mit jeweiliger Dosisreduktion.
- sCAP: Empfehlung zur Gabe von Hydrokortison (Beginn mit 200mg/Tag i.v. Bolus für 7 Tage oder länger mit schrittweiser Dosisreduktion) oder Methylprednisolon (Beginn mit 0,5mg/kg i.v. alle 12h/Tag oder 40mg i.v. Bolus/Tag mit jeweiliger schrittweiser Dosisreduktion). Es wird keine Empfehlung zur Steroidtherapie bei hospitalisierten nicht -intensivpflichtigen CAP -Patienten gegeben.
Abb. 1: Ein praktikabler Algorithmus für den Einsatz von IgM angereicherten intravenösen Immunglobulinen (ivIG) auf Intensivstation. DIC = Disseminierte intravasale Koagulopathie; CLL = chronische lymphatische Leukämie; CVID = variables Immundefektsyndrom. (modifiziert nach M. Ganslmayer, Uniklinikum Erlangen)6
Autor:
Prof. Dr. med. Dr. rer. medic. Adrian Gillissen, Chefarzt der Medizinischen Klinik III, Kreiskliniken am Steinenberg, Am Steinenberg 31, 72764 Reutlingen
_______
1 Ewig S, Kolditz M, Pletz M et al. Behandlung von erwachsenen Patienten mit ambulant erworbener Pneumonie – Update 2021. Pneumologie 2021; 75: 665–729
2 Bogner JR, Gillissen A. Diagnostik und Therapie in der Praxis: Ambulant erworbene Pneumonie. MMW Fortschr Med 2012; 154: 66–75
3 Metlay JP, Waterer GW, Long AC et al. Diagnosis and Treatment of Adults with Community-acquired Pneumonia. An Official Clinical Practice Guideline of the American Thoracic Society and Infectious Diseases Society of America. Am J Respir Crit Care Med 2019; 200: e45–e67
4 Martin-Loeches I, Torres A, Nagavci B et al. ERS/ESICM/ESCMID/ALAT guidelines for the management of severe community-acquired pneumonia. Intensive Care Med 2023; 49: 615–32
5 Torres A, Niederman MS, Chastre J et al. International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia: Guidelines for the management of hospital-acquired pneumonia (HAP)/ventilator-associated pneumonia (VAP) of the European Respiratory Society (ERS), European Society of Intensive Care Medicine (ESICM), European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and Asociación Latinoamericana del Tórax (ALAT). Eur Respir J 2017; 50: 1700582
6 Gillissen A, Jany B, Randerath W: Weissbuch Lunge 2023. Pneumologische Erkrankungen in Deutschland – Zahlen und Fakten. 5. Berlin, Langenhagen: Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin e.V., Deutsche Lungenstiftung e.V.; 2023
7 Ferrer M, Travierso C, Cilloniz C et al. Severe community-acquired pneumonia:
Characteristics and prognostic factors in ventilated and non-ventilated patients. PloS One 2018; 13: e0191721
8 Chaudhuri D, Nei AM, Rochwerg B et al. 2024 Focused Update: Guidelines on Use of Corticosteroids in Sepsis, Acute Respiratory Distress Syndrome, and Community-
Acquired Pneumonia. Crit Care Med 2024; DOI: 10.1097/CCM.0000000000006172
9 Paats MS, Bergen IM, Hanselaar WEJJ et al. Local and systemic cytokine profiles in nonsevere and severe community-acquired pneumonia. Eur Respir J 2013; 41: 1378–85
10 Dequin P-F, Meziani F, Quenot J-P et al. Hydrocortisone in Severe Community-Acquired Pneumonia. N Engl J Med 2023; 388: 1931–41
11 Meduri GU, Shih M-C, Bridges L et al. Low-dose methylprednisolone treatment in
critically ill patients with severe community-acquired pneumonia. Intensive Care Med 2022; 48: 1009–23
12 Cheema HA, Musheer A, Ejaz A et al. Efficacy and safety of corticosteroids for the
treatment of community-acquired pneumonia: A systematic review and meta-analysis of randomized controlled trials. J Crit Care 2024; 80: 154507
13 Wu J-Y, Tsai Y-W, Hsu W-H et al. Efficacy and safety of adjunctive corticosteroids in the treatment of severe community-acquired pneumonia: a systematic review and meta-analysis of randomized controlled trials. Crit Care Lond Engl 2023; 27: 274
14 Saleem N, Kulkarni A, Snow TAC et al. Effect of Corticosteroids on Mortality and Clinical Cure in Community-Acquired Pneumonia: A Systematic Review, Meta-analysis, and Meta-regression of Randomized Control Trials. Chest 2023; 163: 484–97
15 Pletz MW, Blasi F, Chalmers JD et al. International Perspective on the New 2019 American Thoracic Society/Infectious Diseases Society of America Community-Acquired Pneumonia Guideline: A Critical Appraisal by a Global Expert Panel. Chest 2020; 158: 1912–18